Иммунобиологические и патогенетические особенности вирусной диареи крупного рогатого скота
10854
О.В. Сергеев НИИ вирусологии им. Д.И. Ивановского РАМН, Москва
Вирусная диарея (ВД) - высоко контагиозная болезнь, протекающая субклинически, умеренно и остро, с воспалением слизистых оболочек пищеварительного тракта и дыхательных путей. ВД впервые обнаружена и описана в США в середине прошлого века у животных с признаками острой, иногда летальной, диареи и изъязвлением слизистой пищеварительного тракта [25].
В конце прошлого века в Северной Америке и Великобритании были описаны острые вспышки болезни с признаками поражения слизистых оболочек пищеварительного и респираторного трактов среди молочного и мясного скота всех возрастов. У молодых животных развивалась респираторная болезнь и диарея, у взрослых - поражения слизистой ротовой полости и аборты. Смертность наблюдалась, в основном, среди молодняка, и достигала 25-50% [12].
ВД широко распространена в мире и является одной из наиболее сложных проблем инфекционной патологии промышленного скотоводства, причиняющей серьёзный ущерб воспроизводству. Во многих высоко развитых странах заболевание носит эндемичный характер, а серопозитивность взрослого скота достигает 60-80% [23]. Исследование сыворотки крови 1695 животных в 29 штатах США выявило серопозитивность у 57% животных [6]. Во многих странах серопозитивность взрослого скота достигает 50-90% [7, 22]. ВД также широко распространена в Российской Федерации. Так, по данным А.Е. Верховской [1], 90,9% обследованных животных в 15 регионах РФ являются серопозитивными.
Вирусная диарея (ВД) - высоко контагиозная болезнь, протекающая субклинически, умеренно и остро, с воспалением слизистых оболочек пищеварительного тракта и дыхательных путей. ВД впервые обнаружена и описана в США в середине прошлого века у животных с признаками острой, иногда летальной, диареи и изъязвлением слизистой пищеварительного тракта [25].
В конце прошлого века в Северной Америке и Великобритании были описаны острые вспышки болезни с признаками поражения слизистых оболочек пищеварительного и респираторного трактов среди молочного и мясного скота всех возрастов. У молодых животных развивалась респираторная болезнь и диарея, у взрослых - поражения слизистой ротовой полости и аборты. Смертность наблюдалась, в основном, среди молодняка, и достигала 25-50% [12].
ВД широко распространена в мире и является одной из наиболее сложных проблем инфекционной патологии промышленного скотоводства, причиняющей серьёзный ущерб воспроизводству. Во многих высоко развитых странах заболевание носит эндемичный характер, а серопозитивность взрослого скота достигает 60-80% [23]. Исследование сыворотки крови 1695 животных в 29 штатах США выявило серопозитивность у 57% животных [6]. Во многих странах серопозитивность взрослого скота достигает 50-90% [7, 22]. ВД также широко распространена в Российской Федерации. Так, по данным А.Е. Верховской [1], 90,9% обследованных животных в 15 регионах РФ являются серопозитивными.
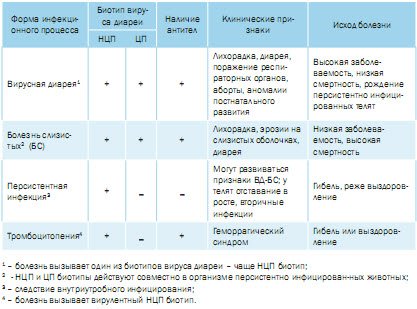
В зависимости от возраста и физиологического состояния животных различают три формы течения болезни: инфекция в постнатальный период; инфекция у стельных коров; персис-тентная инфекция (ПИ) и болезнь слизистых, в основном, у телят. Инфицирование в период стельности сопровождается высоким уровнем абортов, рассасыванием, мумификацией и гибелью плодов, рождением слабых, отстающих в развитии телят [4, 7, 18, 21]. ВД в стадах молочных хозяйствах, обычно, приводит к нарушению репродуктивных функций, снижению продуктивности и заболеванию телят. Желудочно-кишечные и респираторные заболевания молодняка приобретают стационарный характер [18].
Вирус обладает выраженным иммунодепрессивным действием, оказывая неблагоприятное влияние на плодоношение и развитие телят в постанатальный период, способствуя развитию секундарных инфекций [2,3]. В откормочных хозяйствах (фермах) также регистрируют потери поголовья и снижение темпов роста, связанные, в основном, с иммуносуп-рессией [10]. Экономические потери от ВД в США на 1 корову в год составляют от 24 до 200 долларов. Кроме того, к неучтённым потерям относят сокращение генофонда и срока жизни животных [3].
Различают несколько форм течения болезни: острую или собственно вирусную диарею, болезнь слизистых, персистент-ную инфекцию и тромбоцитопению.
Острая форма ВД является результатом первичного инфицирования восприимчивых животных и характеризуется поражениями желудочно-кишечного тракта и респираторных органов, абортами. Клинические признаки заболевания наблюдают преимущественно у животных в возрасте 4-24 месяцев, что связано с присутствием колостральных антител у животных более раннего возраста. У животных старше двух лет болезнь протекает, как правило, субклинически и часто остаётся незамеченной. Наиболее неблагоприятный исход связан с трансплацентарным инфицированием потомства.
Вирус обладает выраженным тропизмом к быстро размножающимся клеткам, особенно к клеткам плода. Трансплацентарное инфицирование плодов в практических условиях происходит достаточно часто. Считается, что у неиммунных стельных коров трансплацентарное инфицирование плодов происходит независимо от стадии стельности с вероятностью 100% [14]. Вирус разных генотипов и соответствующие нейтрализующие антитела обнаружены в сыворотке эмбрионов инфицированных коров [9]. Исход трансплацентарного заражения зависит от иммунологической зрелости плода (125 дней) и вирулентности вируса. Заражение в ранний период стельности приводит к гибели и рассасыванию плода. Заражение на 80-м -125-м дне стельности ведёт к гибели плодов или рождению телят с низкой массой тела или с дефектами развития. Такие телята являются иммунотолерантными, пожизненными носителями и выделителями вируса, предрасположенными к развитию болезни слизистых [7, 16, 23, 24]. Плоды, заражённые после 125 дней стельности, обычно выживают, образуют вируснейтрализующие антитела и освобождаются от вируса [11].
Персистентно инфицированные телята часто рождаются слабыми, отстают в росте и поражаются вторичными пневмониями. Количество ПИ телят может достичь 50%, у которых могут развиться различные клинические признаки болезни слизистых: лихорадка, про-фузная диарея, ринит, эрозивный или язвенный стоматит, истощение и гибель в течение нескольких недель [14, 20]. Постнатальное инфицирование вирусом диареи не приводит к развитию пер-систентной инфекции, у животных наблюдаются клинические признаки и иммунный ответ [15]. ВД легко передаётся от животного к животному, от стада к стаду прямым или непрямым путём, особенно при остром течении и наличии персистентно инфицированных телят, выделяющих вирулентный вирус.
Многообразие клинических форм проявления ВД породили предположения о возможном существовании различных разновидностей возбудителя. Ранние исследования, проведённые в США, выявили существование двух иммунологически различных типов вируса, переболевание которыми не создавало выраженной гетерологичной защиты. Случаи повторных заболеваний, через 4-5 месяцев после реконвалесценции ,свидетельствовали о кратковременности постинфекционного иммунитета или о повторном заражении другим антигенным вариантом вируса ВД, защита против которого, в этот период, была недостаточной [6]. Молекулярно-генетические исследования подтвердили ранние наблюдения и расширили существовавшие представления по этиологии, патогенезу и эпизоотологии ВД, а также способствовало усовершенствованию методов лабораторной диагностики и средств специфической профилактики. Главной особенностью вируса диареи является генотипическое и фенотипическое разнообразие, лежащее в основе полиморфизма клинического проявления болезни и изменения вирулентности и антигенности вируса.
Различают два биотипа вируса: цитопатогенный (ЦП) и нецитопатогенный (НЦП). Каждый биотип вируса существует в виде двух генотипов: 1 и 2 [27, 28], которые различаются между собой генетически и иммунологически [2,3,4,5]. В природе встречаются оба биотипа вируса, относящиеся к первому или второму генотипам.
Генетический анализ различных изолятов вируса диареи выявил тенденцию биотипов и генотипов к мутациям и рекомбинациям, в результате которых происходят внезапные изменения биологических и антигенных свойств [4, 15, 16]. Биотипы классифицируют по их способности вызывать цитопа-тический эффект в культуре клеток, а не по вирулентности для животных. Серологически оба биотипа (ЦП и НЦП) идентичны. Однако в клетках, инфицированных ЦП биотипом синтезируется один дополнительный белок р80, не выявляющийся в клетках, инфицированных НЦП биотипом вируса. Протеин р80 представляет собой небольшую часть крупного неструктурного белка р125, который образуется в клетках, инфицированных любым биотипом вируса. Известно, что оба белка являются вирусными протеазами. Возможно, что р80 в отличие от р125 разрушает важные клеточные белки, вызывая цитопатоген-ное действие [15, 18]. Изменения, приводящие к образованию р80, ответственного за цитопатогенность, обнаружены в геноме ЦП биотипа. Высказано предположение о возможной роли рекомбинации вирусной и клеточной РНК в превращении НЦП биотипа в ЦП биотип. На вероятность превращения НЦП биотипа в ЦП биотип указывает также то, что ЦП вирусы выделяют только в ассоциации с НЦП биотипом [15, 18]. НЦП биотип имеет более широкое распространение, является главной причиной абортов, вызывает персистентную инфекцию и ответственен за поддержание вируса в природе [15]. Хотя болезнь вызывают оба генотипа, но острое и тяжёлое течение вызывает только НЦП вирус типа 2. Выявлено наличие 11 и более субгенотипов вируса [3,5], роль которых в патологии ВД пока не выяснена [3].
Болезнь слизистых с летальным исходом наблюдают, как правило, в возрасте от 6 месяцев до 2-х лет, когда животные, латентно инфицированные НЦП вирусом, суперинфицируются гомологичным ЦП биотипом вируса [15]. Однако ВД с высокой летальностью может быть вызвана НЦП вирусом 2-го генотипа без участия ЦП вируса. Течение болезни может быть острым от 2-х дней до 3-х недель или хроническим, когда животные доживают до 18-месячного возраста [15, 23]. Регистрируют лихорадку, исхудание, обширные эрозии на слизистых оболочках и профузный понос, приводящие к прогрессирующему истощению и гибели [2,3]. Экспериментально болезнь слизистых была воспроизведена у персистентно инфицированного животного путём суперинфицирования ЦП вирусом [8, 17]. В большинстве случаев, при болезни слизистых, спонтанное суперинфицирование ЦП вирусом происходит в результате мутации персис-тирующего в стаде НЦП вируса [2].
Вирулентные НЦП штаммы вируса, вызывающие развитие тромбоцитопении и геморрагической болезни телят, также могут вызывать лихорадку, тяжёлую диарею, геморрагические поражения слизистых и гибель взрослых животных в течение двух недель. Экспериментальное заражение телят НЦП вирусом приводило к развитию тяжёлой тромбоцитопении, геморрагиям, и в ряде случаев к гибели. Тромбоцитопения является результатом прямого разрушающего действия вируса на тромбоциты, а не снижения их продукции в костном мозге. У телят, с титром ВНА в сыворотке крови 1/32 и выше, тромбоцитопе-ния практически не развивалась [13, 18].
Вирус сохраняется в природе, в основном, благодаря наличию персистентно инфицированных (ПИ) животных, которые заражаются НЦП вирусом внутриутробно в течение первых 125 дней стельности. ПИ телята часто рождаются и вырастают внешне здоровыми, однако в их организме вирус продолжает размножаться и постоянно, практически пожизненно, выделяется во внешнюю среду [7, 15,23].
Вирус диареи вызывает атрофию ворсинчатого эпителия двенадцатиперстной кишки, в результате чего развивается энтерит у телят в постнатальном периоде, который может отягощать ротавирусную инфекцию при смешанной инфекции [18]. Поражая лейкоциты и лимфоциты, вирус вызывает иммуносуп-рессию у телят и, тем самым, способствует развитию хронических секундарных инфекций, чаще всего атипичных пневмоний. Вирус может распространяться по всему организму, включая головной мозг, селезёнку, почки, лёгкие и некоторые части кишечника [22]. НЦП биотип вируса диареи инфицирует нейроны коры головного мозга, клетки гипофиза и поджелудочной железы. ЦП биотип вируса чаще выделяют из клеток ретрофарингиальных, мезентериальных, сычужных лимфоузлов, тимуса и Пейеровых бляшек [29]. У взрослых быков вирус может размножаться в клетках тестикулов, персистировать в течение длительного времени (до 2-х лет) и выделяться со спермой [22].
Лабораторная диагностика ВД основывается на использовании различных методов: выделение вируса в культуре клеток с последующей идентификацией (РН, ИФА), обнаружении вирусного генома (ПЦР). Наиболее широко используют методы выявления специфических антител (РН, ИФА) в сыворотке крови и молоке. Без периодического серологического контроля существует вероятность не заметить наличие субклинической инфекции и не предотвратить дальнейшего распространения болезни [2,3].
В неблагополучных хозяйствах, меры предупреждения распространения ВД основываются на выявлении и удалении из стада ПИ животных и усилении иммунитета путём вакцинации. Выявление ПИ животных основывается на клинических признаках и, главным образом, на исследовании образцов крови или молока методом ПЦР [26].
Наличие ПИ носителей вируса среди лактирующих коров, выявляют путём исследования соматических клеток в пробах сборного молока. У молодняка исследуют сыворотку крови или кожный выщип уха, полученный при нумерации. Обычно, для этих целей используют 3 лабораторных метода исследований: выделение вируса в культуре клеток; иммуногистохимический метод и ПЦР [3]. Выявление и удаление из стада ПИ животных является весьма эффективной мерой ликвидации болезни в хозяйстве [15]. Риск инфицирования в откормочных хозяйствах может быть снижен уменьшением плотности популяции животных, а в молочных стадах - разделением животных по возрастным группам [20]. Принято считать, что вакцинация не всегда обеспечивает полноценную защиту от заражения (особенно трансплацентарного), однако вакцинированные животные менее подвержены проявлению острых форм течения ВД и развитию вторичных инфекций.
Защита хозяйств от ВД сводится, прежде всего, к недопущению инфицирования поголовья различными путями. Наиболее опасным путём является ввод в стадо латентно инфицированных животных или использование инфицированной спермы при искусственном осеменении. В США и Канаде, вследствие широкого распространения ВД (уровень серопозитивности) и высокой степени плотности популяций скота, вакцинацию используют как составную часть программы борьбы с ВД.
Меры борьбы с ВД в неблагополучных хозяйствах сводятся к усилению иммунитета, предотвращению риска инфицирования животных (особенно стельных коров) и удалению из стада ПИ носителей вируса [20]. Животные до 6-месячного возраста, перенесшие иммуносупрессию, вследствие острой инфекции становятся очень чувствительными к развитию респираторных болезней. Ситуация значительно осложняется, если они подвергаются воздействию неблагоприятных факторов.
При достаточно тесном контакте практически все животные подвергаются заражению, могут проявлять клинические признаки и популяция чувствительных животных становится частично защищённой. В таких условиях новые случаи заболевания и персистентное инфицирование не происходят и вирус исчезает из стада. Прочный стадный иммунитет при ВД встречается редко потому, что индивидуальный иммунитет является относительным. Более того, стадный иммунитет является преходящим потому, что количество частично иммунных животных в дальнейшем постепенно замещается чувствительными животными. В молочном скотоводстве, где ежегодно обновляется 25% стада, для восстановления полностью чувствительной популяции требуется около 4-х лет. Быстрое удаление частично защищённых животных сокращает это время, а реинфекция или вакцинация продлевают его. Инфицирование отдельных животных может иметь различные последствия и зависит от иммунного статуса животного, вирулентности, дозы вируса, пути заражения, а также от условий кормления и содержания [19].
Специфический иммунитет играет важную роль в борьбе с ВД. Ликвидация ВД без вакцинопрофилактики труднодостижима или невозможна из-за широкой инфицированности, длительного латентного носительства и выделения вируса, высокой численности и плотности поголовья в хозяйстве. Активная иммунизация защищает животных от клинического проявления болезни, но не может защитить от инфицирования и в случае беременности, иногда, может произойти заражение плода с нежелательными последствиями.
Ранее не инфицированные и не вакцинированные серонегативные животные, через 8-10 дней после первичного заражения, образуют сывороточные антитела, титр которых зависит от вирулентности вируса [18]. Антитела, хотя и не защищают от инфицирования, но предупреждают появление выраженных клинических признаков, вызываемых гомологичными или антигенно-родственными штаммами вируса ВД. Гуморальные антитела, приобретённые активно или пассивно, обеспечивают различную степень защиты от болезни. Они являются главным фактором, ограничивающим распространение вируса в стаде. Время исчезновения колостральных антител варьирует от телёнка к телёнку и зависит от начального уровня антител в молозиве и количества потреблённого молозива. У большинства телят, колостральные антитела исчезают к 6-ти месячному возрасту [3]. Животные с низким уровнем антител (особенно колостральных) могут быть инфицированы и активно продуцировать антитела. Низкий уровень антител может быть повышен, также, вакцинацией. Высокий уровень сывороточных антител указывает на выраженную защиту.
Неспособность образования антител может быть связана с приобретённой in utero иммунотолерантностью, либо с иммуносупрессией в результате острого течения болезни. Вак-цинопрофилактика играет важную роль в снижении потерь от ВД. Вакцинация должна защитить от виремии и распространения вируса, предотвратить заражение клеток-мишеней репродуктивной и лимфатической систем, с целью недопущения инфицирования плода и развития иммуносупрессии. С установлением антигенной вариабельности вируса живые и ина-ктивированные вакцины начали готовить из двух генотипов вируса [3, 6]. В США насчитывается более 180 лицензированных вакцин против ВД [3]. В РФ зарегистрировано около 10 вакцин, направленных на защиту от ВД [2].
Применение живых вакцин считается наиболее перспективным, однако опасность таких вакцин связывают с потенциальной абортогенностью многих из них. Вакцины из нескольких штаммов, в т.ч. вирулентных нецитопатогенных, обеспечивают более надёжную иммунологическую защиту [15, 16]. С целью безопасности и эффективности применения живых вакцин рекомендуется всё маточное поголовье вакцинировать не менее чем за 2-3 недели до осеменения для защиты плода от заражения, особенно в течение первой трети стельности [7]. Кроме того, для предотвращения инфицирования и реинфици-рования животных, рекомендуется вакцинировать всё стадо с использованием живых и инактивированных вакцин, по оптимальным схемам их применения. Необходимо также помнить, что высокий уровень антител может нейтрализовать действие живой вакцины. Чтобы избежать интерференции с колостраль-ными антителами живую вакцину следует применять с 6-ти месячного возраста, хотя, вакцинация в более ранний период может быть эффективной у серонегативных телят, а также у телят с небольшим титром антител. Вакцинация в более ранний период требует ревакцинации. Напряжённость и продолжительность иммунитета зависит от частоты естественного инфицирования вакцинированных животных. Применение живой вакцины связано с возможным развитием болезни слизистых после вакцинации. Это состояние напоминает острое течение ВД или болезнь слизистых, проявляющиеся в течение недели после вакцинации, и является часто реакцией на вакцину. Так называемое поствакцинальное заболевание, вероятно, связано с инфицированием вакцинированных животных или является результатом "суперинфицирования" латентно инфицированных животных живой вакциной. Животных, находящихся на откорме, можно прививать живой вакциной после 6-ти месяцев. Инактивированные вакцины безопасны, но их необходимо применять первично дважды и ревакцинировать, по крайней мере, ежегодно.
В ЗАО НПО "НАРВАК" (г. Москва) разработан и производится ряд вакцинных препаратов, предназначенных для специфической профилактики вирусной диареи крупного рогатого скота. Так, вакцины серии "Комбовак", содержащие инакти-вированный вирус диареи, безопасны и рекомендуются для иммунизации стельных коров и нетелей, а также телят с 30-ти дневного возраста.
В некоторых странах Европы вакцинация против ВД запрещена, а программа по оздоровлению основана на выявлении и уничтожении всех инфицированных животных. Во многих европейских странах разрешено использовать только инактивированные вакцины, хотя они не обеспечивают полную защиту от виремии, и сохраняется необходимость выявления и удаления инфицированных животных. Живые вакцины лучше защищают от виремии [3].
Живые вакцины из аттенуированных ЦП штаммов получили широкое применение в ряде стран. Например, во Франции успешно применяется живая вакцина Mucosiffa для иммунизации скота различного возраста, в том числе, стельных коров. В ФРГ живую вакцину применяют для иммунизации скота в неблагополучных хозяйствах. В России живую вакцину ВК-181 N°28 успешно применяют в неблагополучных хозяйствах более 20-ти лет. По эффективности она не уступает французской вакцине Mucosiffa [5]. В последнее время в России применяют комбинированную живую вакцину "Таурус-В" (вакцина ИВП) против инфекционного ринотрахеита, вирусной диареи и парагриппа-3, разработанную ЗАО НПО НАРВАК совместно с EVL лабора-торией (Нидерланды). Эту вакцину применяют для иммунизации животных разного возраста, в том числе коров за 6 недель до осеменения. Аналогичные ограничения существуют при использовании живой вакцины Бови-Шилд-Голд (Ин-тервет).
Анализ данных по специфической профилактике ВД показывает, что успех вакцинации зависит не только от качества вакцин, но и от схемы их применения.
Продукция по теме
Статьи по теме
- Защита здоровья телят в хозяйствах с высокопродуктивным молочным скотом.
- Профилактика болезней копыта у коров
- Респираторные инфекции КРС: классификация рисков для телят на откорм.
- Ящур коров
- Реализация методов по снижению распространения E. coli O157 среди крупного рогатого скота
- Кинематические изменения у молочных коров с индуцированной односторонней хромотой передних конечностей при движении по прямой
- Влияние антропогенного загрязнения на здоровье коров
- Комплексная программа по контролю мастита в молочном животноводстве.
- Диагностика кетозов у коров
- Туберкулез КРС
- Ограничения по использованию тетрациклина в лечении заболеваний копыт коров
- Фолликулярная киста у коров
- Актуальные и новые инфекционные болезни КРС
- 5 советов для обеспечения здоровья новорожденных телят
- Университет штата Канзас разрабатывает новый тест на болезни крупного рогатого скота
- Болезни копыт коров, суставов и кожи
- Причины задержки последа у коров
- Как по молоку коровы определить состояние ее здоровья
- Успех вакцинации или почему телята все равно болеют
- Маститы у высокопродуктивных коров
- Сроки вакцинации влияют на выработку молозива





